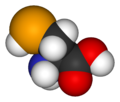
Селеноцистеин
| |||
| Називи | |||
|---|---|---|---|
| IUPAC назив
3-Selanil-2-aminopropanska kiselina
| |||
| Други називи
L-Селеноцистеин; 3-Селанил-L-аланин; Селен цистеин
| |||
| Идентификација | |||
3Д модел (Jmol)
|
|||
| ChEBI | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.236.386 | ||
| КЕГГ[2] | |||
| |||
| Својства | |||
| C3H7NO2Se | |||
| Моларна маса | 168,07 g·mol−1 | ||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25 °C [77 °F], 100 kPa). | |||
| Референце инфокутије | |||
Селеноцистеин (Se-Cys) је аминокиселина која је присутна у више ензима (на пример: глутатионске пероксидазе, тетрајодотиронин 5' дејодиназе, тиоредоксин редуктазе, формат дехидрогеназе, глицин редуктазе, и поједине хидрогеназе).
Номенклатура[уреди | уреди извор]
IUPAC/IUBMB су званично препоручили симболе Sec и U за селеноцистеин.[5]
Структура[уреди | уреди извор]
Селеноцистеин је структурно сличан са цистеином. Један атом селена заузима место сумпора, формирајући селенол групу. Протеини који садрже један или више селеноцистеинских остатака се називају селенопротеинима.
Биологија[уреди | уреди извор]
Селеноцистеин има нижу pKa вредност (5.47) и виши редукциони потенцијал од цистеина. Те особине га чине веома подобним за протеине који учествују у антиоксидантским активностима.[6]
Референце[уреди | уреди извор]
- ^ Сусан Будавари, ур. (2001). Тхе Мерцк Индеx: Ан Енцyцлопедиа оф Цхемицалс, Другс, анд Биологицалс (13тх изд.). Мерцк Публисхинг. ИСБН 0911910131.
- ^ Јоанне Wиxон; Доуглас Келл (2000). „Wебсите Ревиеw: Тхе Кyото Енцyцлопедиа оф Генес анд Геномес — КЕГГ”. Yеаст. 17 (1): 48—55. дои:10.1002/(СИЦИ)1097-0061(200004)17:1<48::АИД-YЕА2>3.0.ЦО;2-Х.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ IUPAC-IUBMB Joint Commission on Biochemical Nomenclature (JCBN) and Nomenclature Committee of IUBMB (NC-IUBMB) (1999). „Newsletter 1999”. European Journal of Biochemistry. 264 (2): 607—609. doi:10.1046/j.1432-1327.1999.news99.x. Архивирано из оригинала (reprint, with permission) 09. 06. 2011. г. Приступљено 06. 01. 2012.
- ^ BJ. Byun & YK. Kang (2011). „Conformational preferences and pK(a) value of selenocysteine residue.”. Biopolymers. 95 (5): 345—53. PMID 21213257. doi:10.1002/bip.21581.
Literatura[уреди | уреди извор]
- F. Zinoni, A. Birkmann, T. C. Stadtman and A. Bock (1986). „Nucleotide sequence and expression of the selenocysteine-containing polypeptide of formate dehydrogenase (formate-hydrogen-lyase-linked) from Escherichia coli”. PNAS. 83 (13): 4650—4654. PMC 323799
 . PMID 2941757. doi:10.1073/pnas.83.13.4650.
. PMID 2941757. doi:10.1073/pnas.83.13.4650. - F. Zinoni, A. Birkmann, W. Leinfelder and A. Bock (1987). „Cotranslational insertion of selenocysteine into formate dehydrogenase from Escherichia coli directed by a UGA codon”. PNAS. 84 (10): 3156—3160. PMC 304827
 . PMID 3033637. doi:10.1073/pnas.84.10.3156.
. PMID 3033637. doi:10.1073/pnas.84.10.3156. - Boyce E. Cone; Rafael Martin Del Rio; Joe Nathan Davis & Thressa C. Stadtman (1976). „Chemical characterization of the selenoprotein component of clostridial glycine reductase: identification of selenocysteine as the organoselenium moiety”. PNAS. 73 (8): 2659—63. PMC 430707
 . PMID 1066676. doi:10.1073/pnas.73.8.2659.
. PMID 1066676. doi:10.1073/pnas.73.8.2659.